Monitoraggio della Spesa Farmaceutica Regionale

E' disponibile sul sito dell'Agenzia Italiana del Farmaco il Monitoraggio della Spesa Farmaceutica Regionale per il periodo Gennaio-Ottobre 2013.

E' disponibile sul sito dell'Agenzia Italiana del Farmaco il Monitoraggio della Spesa Farmaceutica Regionale per il periodo Gennaio-Ottobre 2013.

La redazione di Medscape, un portale di informazione specializzata dedicato a medici e ricercatori, ha stilato una lista delle novità più significative del 2014, grazie all'analisi dei trend emersi dal mondo regolatorio e dalla ricerca nell'anno appena trascorso.

L'Agenzia Italiana del Farmaco, in accordo con l'Agenzia Europea dei Medicinali, rende disponibili nuove ed importanti informazioni su Abraxane (paclitaxel legato all'albumina formulato in nanoparticelle, EU/1/07/428/001-002) e filamenti visibili all'interno della sacca utilizzata per infusione endovenosa.
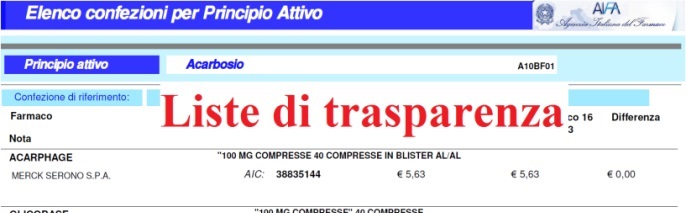
E' stata pubblicata la nuova lista di trasparenza dei medicinali inseriti nell'elenco dei farmaci equivalenti (Legge 178/2002) con i relativi prezzi di riferimento aggiornati al 15 gennaio 2014 comprensivi della riduzione ai sensi della determinazione AIFA 3 luglio 2006, dell'ulteriore riduzione del 5% ai sensi della determinazione A.I.F.A. del 27 settembre 2006 e dell'art.9 comma 1, della Legge 28 febbraio 2008 n.31 (Pay back) e del comma 9 dell'art.11 del D.L.78/2010 convertito con modificazioni dalla Legge del 30 luglio 2010, n.122.

"Un'opinione pubblica bene informata è la nostra Corte Suprema. Perché ad essa ci si può sempre appellare contro le pubbliche ingiustizie, la corruzione, l'indifferenza popolare o gli errori del governo [...]" (Pulitzer).

Il Presidente dell'Agenzia Italiana del Farmaco (AIFA), Prof. Sergio Pecorelli, è intervenuto al Convegno sulla "Sperimentazione animale e diritto alla conoscenza e alla salute",organizzato dalla Commissione Igiene e Sanità del Senato.

La segnalazione di eventi avversi nella pubblicazione di trial clinici in oncologia non è ottimale. E' quanto emerge da una review, sul Journal of Clinical Oncology, che ha esaminato 175 lavori con dati di 96.125 pazienti, pubblicati dal 1 gennaio 2009 al 31 dicembre 2011 su PubMed, Medline ed Embase.

L'Agenzia Italiana del Farmaco (AIFA), in considerazione dell'approssimarsi del picco dell'influenza stagionale previsto per le prossime settimane, ricorda che la più efficace misura di prevenzione è rappresentata dalla vaccinazione annuale.

L'Agenzia Italiana del Farmaco rende disponibili online aggiornamenti relativi al medicinale "Tubertest", non reperibile sul territorio nazionale per il quale è stata autorizzata l'importazione dall'estero su richiesta dell'azienda.

Il Direttore Generale dell'Agenzia Italiana del Farmaco (AIFA), Luca Pani, è intervenuto alla trasmissione "Telecamere Salute" di Rai 3, per illustrare le caratteristiche dei farmaci a base di estratti della cannabis.

La FDA (Food and Drug Administration) ha approvato trametinib in combinazione con dabrafenib per il trattamento di pazienti con melanoma avanzato non rimovibile chirurgicamente o metastatico (in fase avanzata).

L'Agenzia Europea dei Medicinali (EMA) aveva avviato una revisione per due medicinali contenenti stronzio ranelato usati per il trattamento dell'osteoporosi.

La US Food and Drug Administration ha approvato il primo gel sigillante per arrestare la fuoriuscita di fluido dopo l'incisione sulla cornea di pazienti sottoposti ad intervento di cataratta con il posizionamento di una lente intraoculare.

Ai fini di un corretto utilizzo del sistema informativo dei Registri dei farmaci soggetti a monitoraggio, l'Agenzia Italiana del Farmaco, nell'ambito di un progetto di comunicazione periodica con i propri utenti, intende porre l'attenzione su alcuni meccanismi gestionali e di responsabiltà correlati all'utilizzo del proprio account utente e della password di accesso ai sistemi per tutti i profili operativi previsti.

L'Agenzia Italiana del Farmaco, in accordo con l'Agenzia Europea dei Medicinali, rende disponibili nuove ed importanti informazioni sul rischio di errori nel dosaggio di Pixuvri (pixantrone), poiché la dose raccomandata nell'Unione Europea (EU) viene espressa in modo diverso rispetto ad alcuni studi e pubblicazioni.

L'Agenzia Italiana del Farmaco, in accordo con l'Agenzia Europea dei Medicinali, rende disponibili nuove ed importante informazioni riguardo l'errore presente nel paragrafo 3 nel Foglio Illustrativo dei medicinali irbesartan/idroclorotiazide Teva.

La US Food and Drug Administration ha approvato dapaglifozin, farmaco disponibile in compresse per migliorare il controllo glicemico, insieme a dieta ed esercizio fisico, negli adulti con diabete di tipo 2. Farxiga blocca il riassorbimento del glucosio da parte del rene, aumenta l'escrezione del glucosio e abbassa i livelli di glucosio nel sangue.
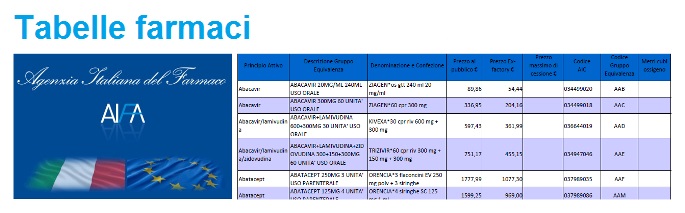
Al fine di consentire la prescrizione per principio attivo disposta dall'articolo 15, comma 11-bis, del decreto legge 6 luglio 2012 n.95, convertito con modificazioni dalla Legge 7 agosto 2012 n. 135, l'Agenzia Italiana del Farmaco rende disponibili per tutti gli Operatori sanitari, le tabelle contenenti l'elenco dei farmaci di fascia A, dispensati dal Servizio sanitario Nazionale, ordinati rispettivamente per principio attivo e per nome commerciale.

L'AIFA, dietro coordinamento della Commissione Europea e dell'EMA e insieme a tutti gli Stati Membri, ha promosso nei mesi scorsi alcune iniziative di sensibilizzazione destinate ai pazienti e agli operatori sanitari per informarli dell'innovazione introdotta dalla nuova legislazione di farmacovigilanza relativa ai medicinali sottoposti a monitoraggio addizionale.

L'aspartame e i suoi prodotti di degradazione sono sicuri per il consumo umano ai livelli di esposizione attuali: queste le conclusioni dell'European Food Safety Authority (EFSA) nella sua prima valutazione completa del rischio dal dolcificante.

E' stato raggiunto lo scorso 20 dicembre in seno al COREPER, il Comitato dei rappresentanti permanenti del Consiglio dell'Unione Europea, l'accordo politico sulle nuove regole da applicare a livello comunitario sulle sperimentazioni cliniche.

Facendo seguito all'ordinanza del Tribunale Ordinario di Torino (N.R.G. 34939/2013), circa l'annullamento dell'efficacia della lista di trasparenza dei medicinali nella parte relativa al principio attivo rivastigmina cerotti, si comunica che è disponibile l'aggiornamento dell'elenco dei prodotti medicinali equivalenti che modifica il precedente elenco pubblicato sul sito AIFA con i prezzi di riferimento aggiornati al 16 dicembre 2013.

L'Agenzia Italiana del Farmaco rende disponibili aggiornamenti relativi al medicinale "Lanitop" (metildigoxin), non reperibile sul territorio nazionale per il quale è stata autorizzata l'importazione dall'estero su richiesta dell'azienda.

Disponibili i dati relativi al primo semestre 2013 sui segnali di farmacovigilanza, nonché la lista delle raccomandazioni espresse dal Comitato di Valutazione dei Rischi per la Farmacovigilanza (PRAC) dell'Agenzia Europea dei Medicinali.

L'Agenzia Italiana del Farmaco, in accordo con l'Agenzia Europea dei Medicinali, rende disponibili nuove informazioni sull'importanza di dimostrare lo stato senza mutazioni (wild type) di RAS (esoni 2, 3 e 4 di KRAS e NRAS) prima del trattamento con Erbitux® (cetuximab).

Pubblicato su Evidence un articolo che descrive i rischi connessi alla polifarmacoterapia negli anziani e propone una riduzione ragionata dei farmaci da somministrare a tali pazienti.
La European Medicines Agency (EMA) e la Food and Drug Administration (FDA) hanno annunciato l'avvio di una iniziativa congiunta per condividere le informazioni relative agli studi di bioequivalenza condotti nell'ambito delle richieste di autorizzazione all'immissione in commercio dei farmaci equivalenti.

Sono 455.000 (ma le stime già parlano di 500.000 ad oggi) gli italiani colpiti finora dall'influenza, secondo i dati inviati all'Istituto Superiore di Sanità dai medici "sentinella" (Medici di Medicina Generale e Pediatri di libera scelta) e raccolti nel database on line Influnet, gestito dal Centro nazionale di epidemiologia, sorveglianza e promozione della salute dell'Istituto.

A soli poco più di quaranta giorni di vita della Banca Dati Farmaci, l'Agenzia Italiana del Farmaco (AIFA) traccia un piccolo bilancio su accessi e contenuti navigati per capire anche il trend di richiesta di notizie inerenti la salute che gli utenti affidano alla rete.

L'Agenzia Italiana del Farmaco rende disponibili aggiornamenti relativi al medicinale "ATGAM (siero antilinfocitario di cavallo) Sterile soluzione 50MG/ML", non reperibile sul territorio nazionale per il quale è stata autorizzata l'importazione dall'estero su richiesta dell'azienda.