XLVI Congresso Nazionale SIFO – Call for Abstract (scad. Oral Presentation 27.05)

Scadenza prossima per la sottomissione delle comunicazioni orali: 27 maggio 2025

Scadenza prossima per la sottomissione delle comunicazioni orali: 27 maggio 2025

La Direzione Generale Salute e Sicurezza Alimentare della Commissione Europea (CE) ha pubblicato gli atti relativi al Webinar sull’ HTA per pazienti ed esperti clinici tenutosi il 16 maggio scorso.

Il capoluogo campano ospiterà RARO TOUR, un evento formativo d’eccellenza dedicato alla gestione delle malattie rare, in programma il 26 e 27 giugno 2025 presso l’Hotel Excelsior – Sala Partenope.

Siamo lieti di annunciarvi che è finalmente online il nuovo sito del Prontuario Galenico!

Nell’ultimo sondaggio effettuato nel 2023, il 95% dei farmacisti ospedalieri identifica le carenze di medicinali e dispositivi medici come una seria preoccupazione, nonostante i loro sforzi per mitigarle. Per continuare ad affrontare questo problema a livello europeo, EAHP da’ eco al bisogno di dati concreti e quanto più’ attuali da raccogliere per essere sottoposti ai decisori politici ed altre istituzioni che si interessano di questa criticità.

E' stata pubblicata la nuova lista di trasparenza dei medicinali inseriti nell'elenco dei farmaci equivalenti (Legge 178/2002) con i relativi prezzi di riferimento aggiornati al 15 maggio 2025.

L’Agenzia Europea del Farmaco (EMA) ha pubblicato le raccomandazioni per l’aggiornamento dei vaccini COVID-19 alle nuove varianti in circolazione.

Il Consiglio di Amministrazione dell’Agenzia Italiana del Farmaco (AIFA), nella seduta del 14 maggio, ha approvato l’ammissione alla rimborsabilità da parte del Servizio Sanitario Nazionale (SSN) di undici farmaci, tra cui un medicinale orfano, quattro nuove entità chimiche, due generici, un farmaco di importazione parallela e tre estensioni di indicazioni terapeutiche.

Si comunica che è stata revocata l'autorizzazione all'immissione in commercio o disposto il ritiro di lotti dei medicinali di seguito indicati.

L’EMA ha pubblicato il resoconto della riunione del 5-8 maggio 2025 del Comitato per la Valutazione del Rischio di Farmacovigilanza (PRAC).

Avviso dell'Agenzia Italiana del Farmaco sul furto di farmaci avvenuto presso la farmacia territoriale di Lagonegro (PZ).
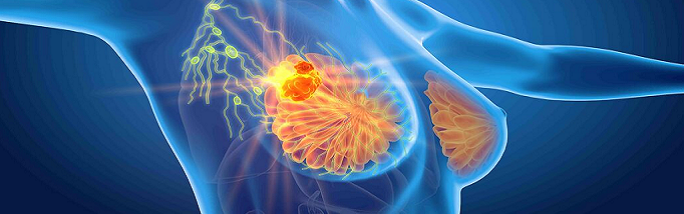
Nota Informativa Importante di sicurezza concordata con le autorità regolatorie europee e l’Agenzia Italiana del Farmaco (AIFA) diretta agli operatori sanitari per informare in merito alle nuove condizioni di conservazione ed il nuovo periodo di validità di ribociclib.
Kisqali (ribociclib) è indicato per il trattamento del carcinoma mammario HR positivo e HER2 negativo, sia in stadio localmente avanzato/metastatico sia, più recentemente, in fase iniziale ad alto rischio di recidiva. Le nuove condizioni di conservazione e di validità si applicano a tutte le indicazioni.
Le informazioni sul prodotto sono state aggiornate per riflettere queste modifiche.
Per ulteriori informazioni:
Nota Informativa Importante su Kisqali (ribociclib)
Fonte:www.aifa.gov.it
Redazione SifoWeb

ROMA, 13 MAGGIO - E’ stata presentata nei giorni scorsi a Roma e presso il Festival della Robotica di Pisa la Call to Action “Per lo sviluppo e la valorizzazione della chirurgia robotica in Italia”, iniziativa multidisciplinare nata per promuovere un confronto tecnico-scientifico e istituzionale sul futuro di una delle tecnologie più avanzate in ambito sanitario.

L'AIFA aggiorna l'elenco dei medicinali che, a giudizio della Commissione Scientifica ed Economica, possiedono il requisito di innovatività terapeutica piena o condizionata.

SIFO comunica a tutti i soci l’apertura dell’avviso di selezione per il conferimento degli incarichi di Coordinatore e Collaboratore delle Aree Scientifico-Culturali (ASC) per il quadriennio 2024–2028.
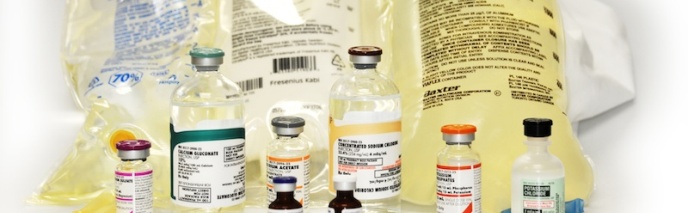
Formazione per farmacisti ospedalieri: qualità e sicurezza nell’allestimento delle terapie nutrizionali.
Il 13 e 14 giugno 2025, ad Ancona, un corso intensivo riservato ai Soci SIFO approfondisce le fasi critiche della nutrizione parenterale personalizzata, con focus sul ruolo centrale del farmacista.

L'EMA e i Direttori delle Agenzie per i Medicinali (HMA) hanno pubblicato un piano di lavoro congiunto "Data and AI in medicines regulation to 2028" per ottimizzare l'uso dei dati e dell'intelligenza artificiale (AI).

E' stato pubblicato sul BURT l'avviso relativo alle tre borse di studio relative al progetto: "Sistema di Farmacovigilanza Regionale - La Sicurezza dei Farmaci, vaccini e Dispositivi Medici nell'Azienda Usl Toscana Sud Est".

Si comunica che è stata revocata l'autorizzazione all'immissione in commercio o disposto il ritiro di lotti dei medicinali di seguito indicati.

ROMA, 5 maggio - Il 5 maggio ricorre la Giornata mondiale dell'igiene delle mani, ricorrenza istituita dall'Organizzazione Mondiale della Sanità con lo scopo di sensibilizzare gli operatori sanitari ed i cittadini sull'importanza di attuare sempre una corretta igiene delle mani quale pratica imprescindibile di prevenzione e controllo delle infezioni.
L’Agenzia pubblica i report sul monitoraggio dei farmaci biosimilari in Italia, aggiornati a dicembre 2024.

OMS rilancia l’allerta internazionale. Il Ministero aggiorna le linee guida, SIFO continua il monitoraggio scientifico.

L'Organizzazione per la Cooperazione e lo Sviluppo Economico (OCSE) ha pubblicato l’Health Working Papers No. 177 “Towards identifying good practices in the assessment of digital medical devices: Insights from several OECD countries ”.

Si comunica che è stata revocata l'autorizzazione all'immissione in commercio o disposto il ritiro di lotti dei medicinali di seguito indicati.
L’intelligenza artificiale e le tecnologie digitali stanno rivoluzionando la Sanità. Il corso, rivolto ai professionisti del SSN, fornisce strumenti concreti per affrontare questa transizione con competenze aggiornate, analizzando aspetti normativi, gestionali e regolatori. Appuntamento a Roma l’11 giugno 2025.

L’Organizzazione Mondiale della Sanità (OMS) ha pubblicato la relazione “Global Antimicrobial Resistance and Use Surveillance System (GLASS) report. Antibiotic use data for 2022”.

Nota Informativa Importante concordata con le autorità regolatorie europee e l’Agenzia Italiana del Farmaco (AIFA) diretta agli operatori sanitari per informare in merito alla presenza in ruxolitinib crema di piccole particelle visibili simili a cristalli che non comportano alcun rischio significativo di sicurezza per i pazienti, né si prevede che impattino l'efficacia del prodotto.
Opzelura (ruxolitinib) è indicato per il trattamento della vitiligine non segmentale con interessamento facciale negli adulti e negli adolescenti a partire dai 12 anni di età.
La causa precisa all’origine della formazione dei cristalli non è chiara. Durante la produzione di Opzelura potrebbero formarsi delle particelle dal principio attivo (ruxolitinib, come fosfato). In caso di formazione di ruxolitinib diidrato, questo potrebbe presentarsi sotto forma di piccole particelle nella crema.
Per ulteriori informazioni:
Nota Informativa Importante su Opzelura (ruxolitinib)
Fonte:www.aifa.gov.it
Redazione SifoWeb

Si informano gli utenti dei Registri dei Farmaci sottoposti a Monitoraggio che a partire dal 25/04/2025 è possibile utilizzare, in regime di rimborsabilità SSN, il medicinale a base di talazoparib per una nuova indicazione terapeutica.

L’EMA ha pubblicato le raccomandazioni adottate nella riunione del 22-25 aprile dal Comitato per i Prodotti Medicinali per Uso Umano (CHMP)

Si comunica che è stata revocata l'autorizzazione all'immissione in commercio o disposto il ritiro di lotti dei medicinali di seguito indicati.